Preview Mode
You're viewing this material in preview mode. Sign up to track your progress and access all features.
K4-B1 (R). Dualizm falowo-cząstkowy; fotony; zależność \(E=hf\)
In Progress
# K4-B1 (R). Dualizm falowo-cząstkowy; fotony; zależność \(E=hf\)
Ta lekcja dotyczy **zakresu rozszerzonego (R)**.
Poniższa ilustracja pokazuje, dlaczego w fizyce kwantowej światło opisujemy dwiema perspektywami: jako falę w doświadczeniach interferencyjnych i jako strumień fotonów w zjawiskach wymiany energii.
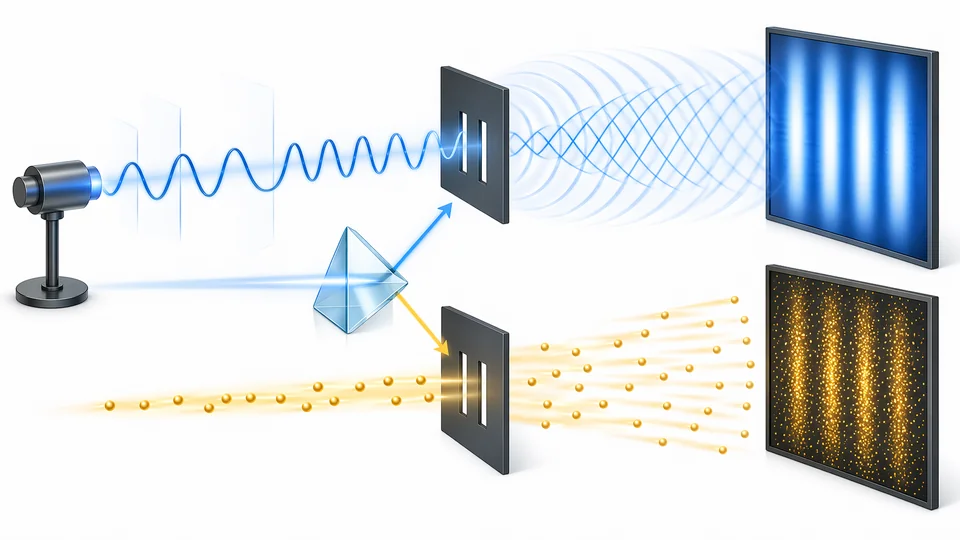
## Cel lekcji
Po tej lekcji potrafisz:
- wyjaśnić, na czym polega **dualizm falowo-cząstkowy** światła,
- opisać foton jako kwant promieniowania elektromagnetycznego,
- obliczać energię fotonu \(E=hf=\frac{hc}{\lambda}\) i jego pęd \(p=\frac{h}{\lambda}\),
- rozróżniać rolę częstotliwości i natężenia w modelu kwantowym.
---
## 1) Co oznacza „dualizm”?
Światło wykazuje:
- własności **falowe** (interferencja, dyfrakcja),
- własności **cząstkowe** (zjawiska, w których energia jest przekazywana porcjami).
Nie oznacza to, że „raz jest falą, raz cząstką” w sposób dowolny. Oznacza, że do opisu różnych doświadczeń potrzebujemy różnych modeli.
---
## 2) Problem klasyczny: promieniowanie ciała doskonale czarnego (intuicja)
W fizyce klasycznej przewidywano błędny rozkład energii promieniowania (tzw. „katastrofa w nadfiolecie”).
Planck zaproponował, że energia promieniowania jest emitowana/absorbowana w porcjach — **kwantach**.
---
## 3) Foton i energia \(E=hf\) (R)
Foton to kwant promieniowania elektromagnetycznego.
Energia fotonu:
\[E = hf.\]
Gdzie:
- \(h\) — stała Plancka,
- \(f\) — częstotliwość fali.
Ponieważ \(c=\lambda f\), często wygodniej:
\[E=\frac{hc}{\lambda}.\]
W praktyce maturalnej bardzo często używa się przybliżenia:
\[hc\approx 1240\,\text{eV·nm}.\]
Wtedy dla \(\lambda\) w nm dostajesz \(E\) w eV:
\[E(\text{eV})\approx \frac{1240}{\lambda(\text{nm})}.\]
---
## 4) Pęd fotonu (R)
Mimo że foton nie ma masy spoczynkowej, ma pęd:
\[p=\frac{E}{c}=\frac{hf}{c}=\frac{h}{\lambda}.\]
To jest ważne np. dla ciśnienia promieniowania i dla pełnego obrazu fotoefektu.
---
## 5) Natężenie vs częstotliwość — co „robi co”?
W modelu kwantowym:
- **częstotliwość** (czyli \(\lambda\)) decyduje o energii pojedynczego fotonu,
- **natężenie** (intensywność) decyduje głównie o liczbie fotonów docierających w jednostce czasu.
To bardzo ważne rozróżnienie:
- można mieć wiele „słabych” fotonów (mała energia),
- albo mało „mocnych” fotonów (duża energia).
---
## 6) Przykłady
### Przykład 1: energia fotonu światła zielonego
\(\lambda=500\,\text{nm}\):
\[E\approx \frac{1240}{500}\,\text{eV}\approx 2{,}48\,\text{eV}.\]
### Przykład 2: porównanie UV i IR
- UV ma mniejszą \(\lambda\) → większą energię fotonu,
- IR ma większą \(\lambda\) → mniejszą energię fotonu.
---
## Najczęstsze błędy
1) Mylenie: „większe natężenie” = „większa energia fotonu” (to nie to).
2) Gubienie jednostek \(\lambda\): nm vs m.
3) Zapominanie, że \(E\propto f\) i \(E\propto 1/\lambda\).
---
## Ćwiczenia do samodzielnej pracy (z odpowiedziami)
1) Oblicz energię fotonu dla \(\lambda=400\,\text{nm}\) (w eV).
2) Które fotony mają większą energię: \(\lambda=300\,\text{nm}\) czy \(\lambda=700\,\text{nm}\)?
3) (R) Zapisz wzór na pęd fotonu w funkcji \(\lambda\).
**Odpowiedzi:**
1) \(E\approx 1240/400\approx 3{,}10\,\text{eV}\). 2) \(300\,\text{nm}\). 3) \(p=h/\lambda\).
---
## Wizualizacje
### Energia fotonu a długość fali (zadaniowo)
\(E\,[\text{eV}]\approx 1240/\lambda\,[\text{nm}]\).
[[graph expr="1240/x" domain="300,900" height="260"]]
### Natężenie vs częstotliwość (intuicja)
Natężenie zwiększa liczbę fotonów, ale energia pojedynczego fotonu zależy od \(\lambda\) (czyli od \(f\)).
[[canvas renderer="bar-chart" width="720" height="260"]]
{
"version": 1,
"data": [
{"label": "energia 1 fotonu", "value": 1, "color": "#5e35b1"},
{"label": "liczba fotonów", "value": 3, "color": "#1565c0"}
],
"xAxis": {"label": "co zmieniasz"},
"yAxis": {"label": "efekt (schemat)"}
}
[[/canvas]]
